- ผู้เขียน Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:51.
- แก้ไขล่าสุด 2025-06-01 07:38.
ความแตกต่างที่สำคัญ - ลิแกนด์ที่แข็งแกร่ง vs ลิแกนด์ที่อ่อนแอ
ลิแกนด์คืออะตอม ไอออน หรือโมเลกุลที่บริจาคหรือแบ่งอิเล็กตรอนสองตัวผ่านพันธะโควาเลนต์ประสานกับอะตอมหรือไอออนตรงกลาง แนวคิดของลิแกนด์ถูกกล่าวถึงภายใต้เคมีประสานงาน แกนด์เป็นสารเคมีที่เกี่ยวข้องกับการก่อตัวของสารประกอบเชิงซ้อนที่มีไอออนของโลหะ ดังนั้นจึงเรียกอีกอย่างว่าสารก่อเชิงซ้อน ลิแกนด์สามารถเป็นโมโนเดนเทท ไบเดนเทท ตรีศูล ฯลฯ ขึ้นอยู่กับลักษณะฟันของแกนด์ Denticity คือจำนวนกลุ่มผู้บริจาคที่มีอยู่ในลิแกนด์ Monodentate หมายความว่าลิแกนด์มีกลุ่มผู้บริจาคเพียงกลุ่มเดียว Bidentate หมายความว่ามีกลุ่มผู้บริจาคสองกลุ่มต่อหนึ่งโมเลกุลลิแกนด์ลิแกนด์มีสองประเภทหลักที่จัดประเภทตามทฤษฎีสนามคริสตัล แกนด์ที่แข็งแกร่ง (หรือแกนด์สนามที่แข็งแกร่ง) และแกนด์ที่อ่อนแอ (หรือแกนด์สนามที่อ่อนแอ) ความแตกต่างที่สำคัญระหว่างแกนด์ที่แข็งแกร่งและแกนด์ที่อ่อนแอคือการแยกออร์บิทัลหลังจากจับกับลิแกนด์สนามที่แข็งแกร่งทำให้เกิดความแตกต่างที่สูงขึ้นระหว่างออร์บิทัลระดับพลังงานที่สูงขึ้นและต่ำ ในขณะที่การแยกออร์บิทัลหลังจากจับกับลิแกนด์สนามที่อ่อนแอทำให้เกิดความแตกต่างที่ต่ำกว่า ระหว่างวงโคจรระดับพลังงานสูงและต่ำ
ทฤษฎีสนามคริสตัลคืออะไร
ทฤษฎีสนามคริสตัลสามารถอธิบายได้ว่าเป็นแบบจำลองที่ออกแบบมาเพื่ออธิบายการแตกของความเสื่อม (เปลือกอิเล็กตรอนที่มีพลังงานเท่ากัน) ของออร์บิทัลอิเล็กตรอน (โดยปกติคือ d หรือ f orbitals) เนื่องจากสนามไฟฟ้าสถิตที่เกิดจากสภาพแวดล้อม แอนไอออนหรือแอนไอออน (หรือลิแกนด์) ทฤษฎีนี้มักใช้เพื่อแสดงพฤติกรรมของสารประกอบเชิงซ้อนของไอออนโลหะทรานซิชัน ทฤษฎีนี้สามารถอธิบายคุณสมบัติของแม่เหล็ก สีของคอมเพล็กซ์การประสานงาน เอนทัลปีไฮเดรชั่น ฯลฯ
ทฤษฎี:
ปฏิกิริยาระหว่างไอออนของโลหะกับลิแกนด์เป็นผลมาจากแรงดึงดูดระหว่างไอออนของโลหะที่มีประจุบวกและประจุลบของอิเล็กตรอนที่ไม่ได้รับการจับคู่ของลิแกนด์ ทฤษฎีนี้มีพื้นฐานมาจากการเปลี่ยนแปลงที่เกิดขึ้นในออร์บิทัลอิเล็กตรอนที่เสื่อมทรามห้าวงเป็นส่วนใหญ่ (อะตอมของโลหะมีออร์บิทัลห้า d) เมื่อลิแกนด์เข้าใกล้โลหะไอออน อิเล็กตรอนที่ไม่มีคู่จะอยู่ใกล้กับออร์บิทัลบางตัวมากกว่าออร์บิทัล d อื่นของไอออนโลหะ ทำให้สูญเสียความเสื่อมโทรม นอกจากนี้ อิเล็กตรอนใน d orbitals ขับไล่อิเล็กตรอนของลิแกนด์ (เพราะทั้งคู่มีประจุลบ) ดังนั้น d ออร์บิทัลที่อยู่ใกล้กับลิแกนด์จึงมีพลังงานสูงกว่าออร์บิทัล d อื่น ส่งผลให้มีการแยก d ออร์บิทัลออกเป็นออร์บิทัล d พลังงานสูงและออร์บิทัล d พลังงานต่ำ โดยพิจารณาจากพลังงาน
ปัจจัยบางประการที่ส่งผลต่อการแยกส่วนนี้คือ; ลักษณะของโลหะไอออน สถานะออกซิเดชันของไอออนของโลหะ การจัดเรียงตัวของลิแกนด์รอบไอออนของโลหะตรงกลาง และลักษณะของลิแกนด์หลังจากการแยกออร์บิทัล d เหล่านี้ตามพลังงาน ความแตกต่างระหว่างออร์บิทัล d พลังงานสูงและต่ำเรียกว่าพารามิเตอร์การแยกสนามคริสตัล (∆oct สำหรับคอมเพล็กซ์แปดด้าน)
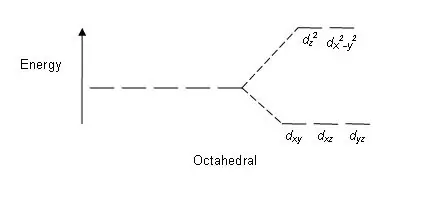
รูปที่ 01: รูปแบบการแยกในคอมเพล็กซ์แปดด้าน
รูปแบบการแยก: เนื่องจากมีออร์บิทัลห้า d การแยกจึงเกิดขึ้นในอัตราส่วน 2:3 ในคอมเพล็กซ์แปดด้าน ออร์บิทัลสองออร์บิทัลอยู่ในระดับพลังงานสูง (เรียกรวมกันว่า ‘เช่น’) และออร์บิทัลสามออร์บิทัลอยู่ในระดับพลังงานที่ต่ำกว่า (รวมเรียกว่า t2g) ในเชิงซ้อนจัตุรมุข ตรงกันข้ามเกิดขึ้น; ออร์บิทัลสามออร์บิทัลอยู่ในระดับพลังงานที่สูงขึ้นและอีกสองออร์บิทัลอยู่ในระดับพลังงานที่ต่ำกว่า
สตรองลิแกนด์คืออะไร
แกนด์ที่แข็งแกร่งหรือแกนด์สนามที่แข็งแกร่งคือแกนด์ที่สามารถส่งผลให้มีการแยกสนามผลึกที่สูงขึ้นซึ่งหมายความว่าการผูกมัดของแกนด์สนามที่แข็งแกร่งทำให้เกิดความแตกต่างที่สูงขึ้นระหว่างออร์บิทัลระดับพลังงานที่สูงขึ้นและต่ำลง ตัวอย่าง ได้แก่ CN- (ไซยาไนด์ลิแกนด์), NO2- (ไนโตรลิแกนด์) และ CO (คาร์บอนิล ลิแกนด์).
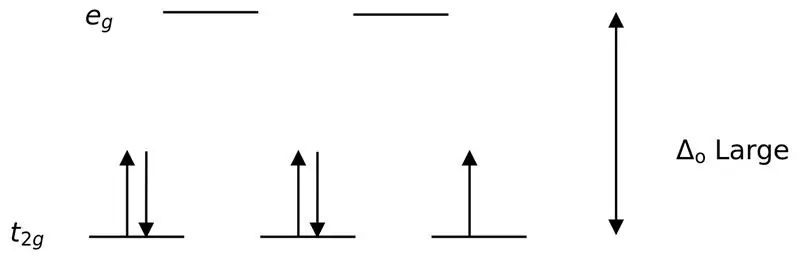
รูปที่ 02: สปินต่ำ
ในการก่อตัวของสารเชิงซ้อนที่มีแกนด์เหล่านี้ ในตอนแรก ออร์บิทัลพลังงานต่ำกว่า (t2g) จะถูกเติมด้วยอิเล็กตรอนทั้งหมดก่อนที่จะเติมออร์บิทัลระดับพลังงานสูงอื่นๆ (เช่น) คอมเพล็กซ์ที่เกิดขึ้นในลักษณะนี้เรียกว่า "คอมเพล็กซ์การหมุนต่ำ"
ลิแกนด์ที่อ่อนแอคืออะไร
แกนด์ที่อ่อนแอหรือแกนด์สนามที่อ่อนแอเป็นแกนด์ที่อาจส่งผลให้มีการแยกสนามผลึกที่ต่ำกว่า ซึ่งหมายความว่าการผูกมัดของแกนด์สนามที่อ่อนแอทำให้เกิดความแตกต่างที่ต่ำกว่าระหว่างออร์บิทัลระดับพลังงานที่สูงขึ้นและต่ำลง
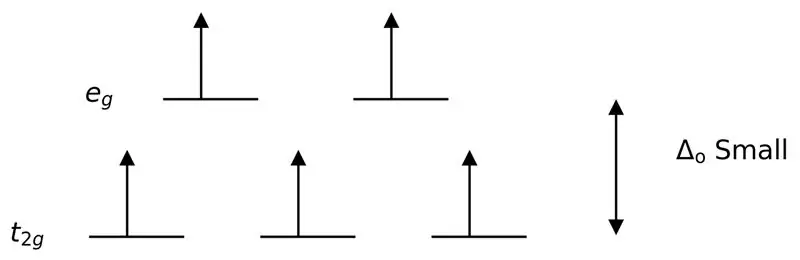
รูปที่ 3: High Spin Splitting
ในกรณีนี้ เนื่องจากความแตกต่างที่ต่ำระหว่างระดับการโคจรทั้งสองทำให้เกิดแรงผลักระหว่างอิเล็กตรอนในระดับพลังงานเหล่านั้น ออร์บิทัลที่มีพลังงานสูงกว่าจึงสามารถเติมอิเล็กตรอนได้ง่ายเมื่อเทียบกับออร์บิทัลที่มีพลังงานต่ำ คอมเพล็กซ์ที่สร้างด้วยลิแกนด์เหล่านี้เรียกว่า "คอมเพล็กซ์สปินสูง" ตัวอย่างของแกนด์สนามที่อ่อนแอ ได้แก่ I- (ลิแกนด์ไอโอไดด์), Br- (โบรไมด์ลิแกนด์) เป็นต้น
ลิแกนด์ที่แข็งแกร่งและลิแกนด์ที่อ่อนแอคืออะไร
ลิแกนด์ที่แข็งแกร่ง vs ลิแกนด์ที่อ่อนแอ |
|
| แกนด์ที่แข็งแกร่งหรือแกนด์สนามที่แข็งแกร่งคือแกนด์ที่สามารถส่งผลให้มีการแยกสนามผลึกที่สูงขึ้น | แกนด์อ่อนหรือแกนด์สนามอ่อนคือแกนด์ที่ส่งผลให้สนามผลึกแตกต่ำลง |
| ทฤษฎี | |
| การแยกตัวหลังจากผูกแกนด์สนามที่แข็งแกร่งทำให้เกิดความแตกต่างที่สูงขึ้นระหว่างออร์บิทัลระดับพลังงานสูงและต่ำ | การแยกออร์บิทัลหลังจากผูกแกนด์สนามที่อ่อนแอทำให้เกิดความแตกต่างที่ต่ำกว่าระหว่างออร์บิทัลระดับพลังงานสูงและต่ำ |
| Category | |
| คอมเพล็กซ์ที่สร้างด้วยแกนด์สนามที่แข็งแกร่งเรียกว่า “คอมเพล็กซ์สปินต่ำ” | คอมเพล็กซ์ที่สร้างด้วยแกนด์สนามที่อ่อนแอเรียกว่า “คอมเพล็กซ์การหมุนสูง” |
สรุป - ลิแกนด์ที่แข็งแกร่ง vs ลิแกนด์ที่อ่อนแอ
ลิแกนด์ที่แข็งแรงและลิแกนด์ที่อ่อนแอคือแอนไอออนหรือโมเลกุลที่ทำให้เกิดการแยกออร์บิทัลของไอออนโลหะออกเป็นสองระดับพลังงานความแตกต่างระหว่างแกนด์ที่แข็งแกร่งและแกนด์ที่อ่อนแอคือการแยกตัวหลังจากผูกแกนด์สนามที่แข็งแรงทำให้เกิดความแตกต่างที่สูงขึ้นระหว่างออร์บิทัลระดับพลังงานที่สูงขึ้นและต่ำในขณะที่การแยกออร์บิทัลหลังจากจับกับลิแกนด์สนามที่อ่อนแอทำให้เกิดความแตกต่างที่ต่ำกว่าระหว่างระดับที่สูงขึ้นและต่ำ ออร์บิทัลระดับพลังงาน

